
¿Qué es RADIAL?
RADIAL es un estudio de investigación científica. El objetivo de RADIAL es probar una nueva forma de investigación científica que pueda reducir la carga que supone participar en estudios clínicos. Queremos comprobar si los llamados ensayos clínicos descentralizados funcionan igual de bien que los ensayos clínicos tradicionales. Los ensayos tradicionales se llevan a cabo en hospitales o en clínicas. En los ensayos descentralizados, las personas participan desde sus casas empleando tecnologías modernas como aparatos y herramientas de teleconferencia, sin tener que desplazarse para acudir a las visitas en el hospital.
RADIAL está dividido en dos partes. Una parte pondrá a prueba el enfoque de los estudios clínicos descentralizados y la otra el enfoque tradicional y un enfoque híbrido. El enfoque híbrido combina elementos tanto de los estudios clínicos tradicionales como de los descentralizados.
Este formato aporta información únicamente sobre la parte descentralizada del estudio RADIAL.
El estudio está dirigido por el Centro Médico Universitario de Utrecht en los Países Bajos. Lo ha preparado Trials@Home, un grupo internacional de más de 30 socios. El estudio está financiado por la Empresa Común para la Iniciativa sobre Medicamentos Innovadores 2.
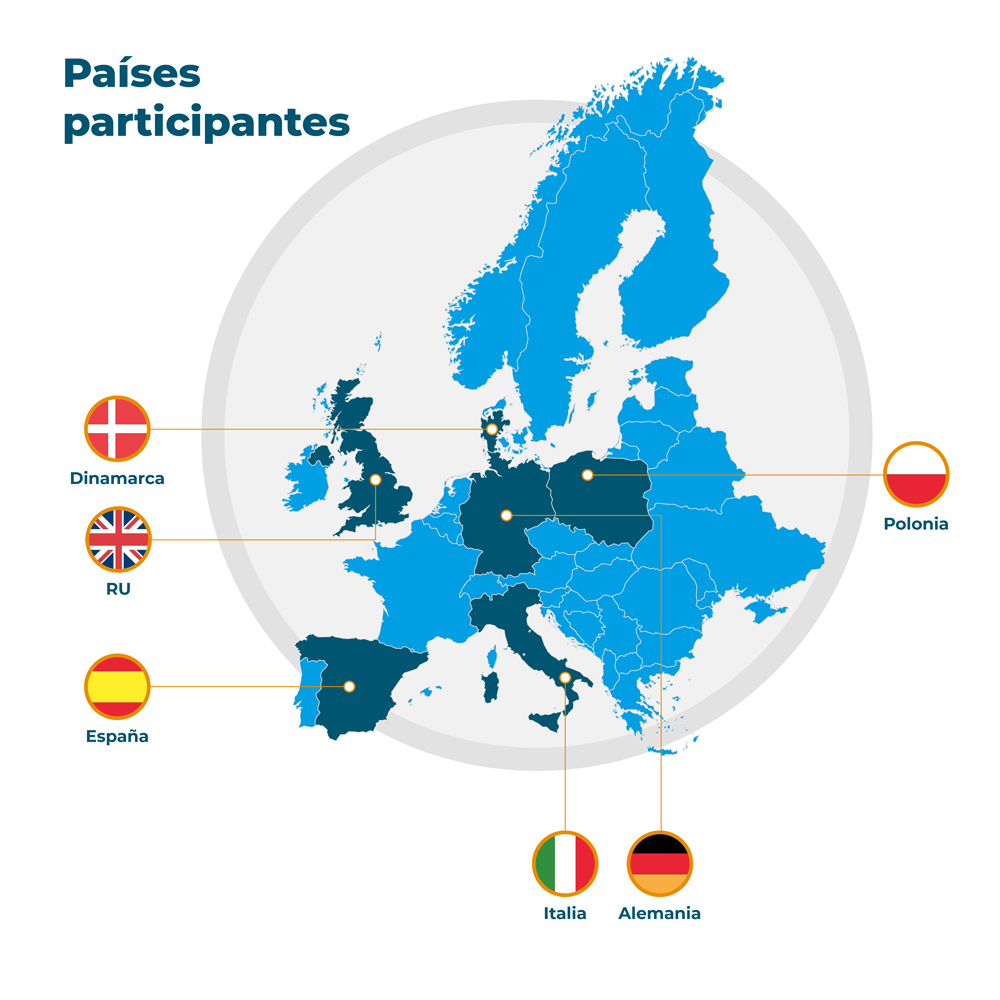
El estudio se lleva a cabo en 6 países europeos. Participará un total de 600 personas.
¿Quién puede participar en el estudio?
El ensayo RADIAL está abierto a personas mayores de 18 años que padecen diabetes tipo 2 desde hace al menos un año y que reciben insulina basal de larga duración.
La diabetes tipo 2 es el objeto de estudio del ensayo RADIAL porque gran parte de su manejo se lleva a cabo en el hogar y es una afección adecuada para la atención médica remota mediante el uso de tecnología.
Las personas que estén embarazadas, en período de lactancia o planeando quedarse embarazadas no podrán participar. Las mujeres menores de 60 deberán hacerse una prueba de embarazo en orina.
¿Qué le ocurrirá a usted si participa?
El estudio consta de 2 períodos: un período de selección de 3 a 6 semanas y un período de tratamiento de 6 meses. En el periodo de selección, comprobaremos si RADIAL es adecuado para usted y si puede participar con seguridad en el estudio. Si le invitamos a continuar en el estudio tras el período de selección, empezará a utilizar la insulina llamada Toujeo® en vez de su insulina basal actual.
La dosis, la fecha y la hora de cada inyección de Toujeo® se registra automáticamente mediante una «tapa inteligente» en la pluma de inyección. Usted se medirá el peso, la presión arterial y la frecuencia cardíaca, y se tomará algunas muestras de sangre para determinar su nivel de HbA1c. También registrará los niveles de glucosa en sangre mediante automediciones diarias empleando punciones en el dedo y un medidor de la glucosa en sangre. Registrará cualquier episodio de hipoglucemia u otros efectos secundarios que puedan darse en un diario electrónico.
Usted recibirá todo el material que necesita para el estudio en su domicilio. Esto incluye un glucómetro y el material relacionado (lancetas, tiras de prueba de glucosa, etc.), un aparato de monitorización de la presión arterial, la pluma precargada de insulina con la nueva insulina basal y las agujas. Recibirá formación sobre cómo utilizarlo. Todo el contacto con el equipo del estudio se hará mediante videollamadas o por teléfono.
Al inicio del estudio, instalará una segunda aplicación del estudio en su smartphone o tablet. Recibirá instrucciones detalladas sobre la instalación más adelante si elige participar en RADIAL.
La siguiente figura muestra los procedimientos principales del estudio.
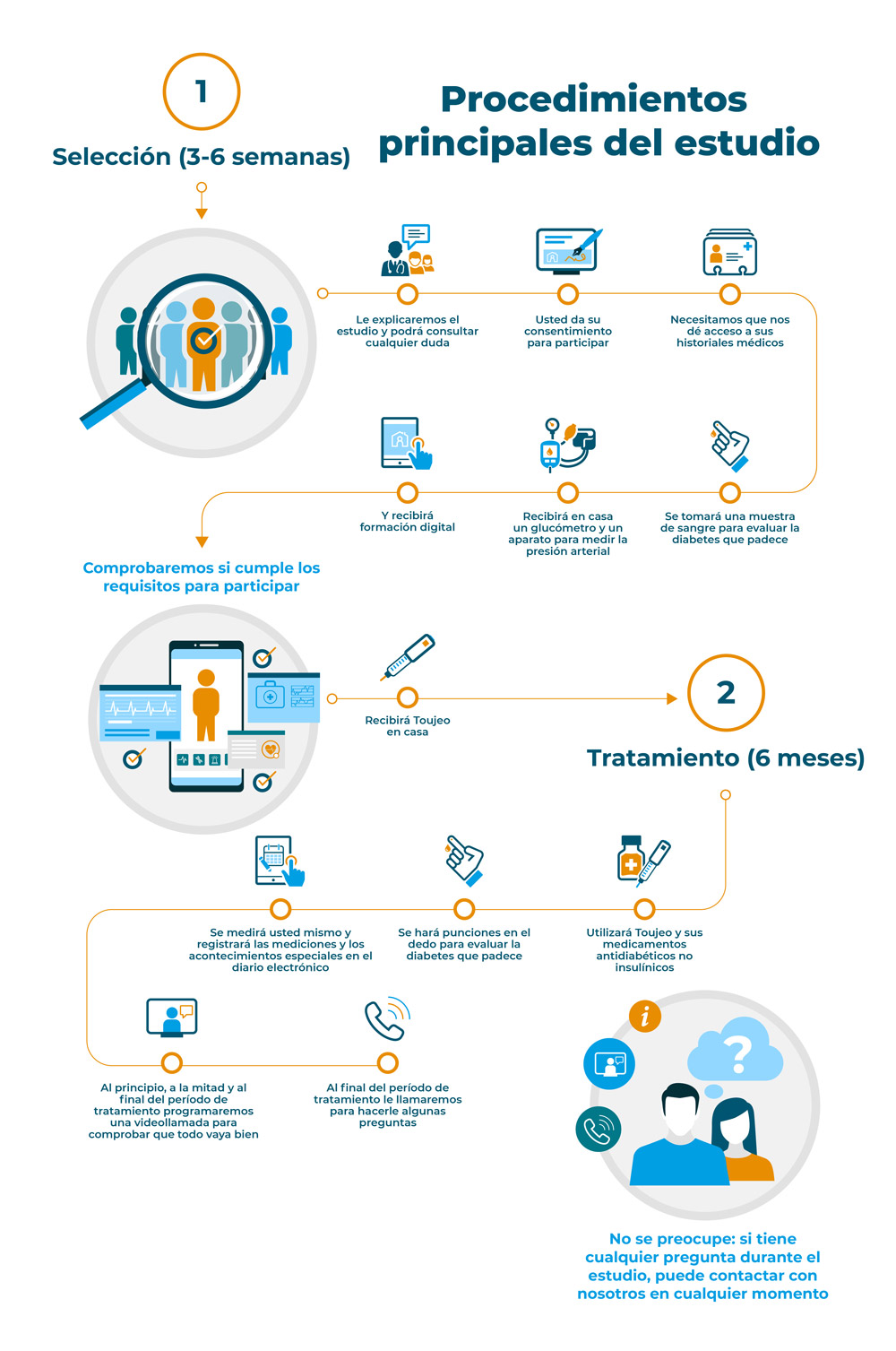
¿Qué medicación recibirá?
La insulina basal que utilizará durante el estudio es Toujeo® (insulina glargina 300 U/ml). Toujeo® es un tratamiento aprobado para mejorar el control de la glucosa en personas a partir de los 6 años de edad que viven con diabetes de tipo 2. Se suministra en una pluma precargada desechable llamada Toujeo® SoloStar. Usted se puede inyectar Toujeo® bajo la piel en la parte delantera de los muslos, en la zona superior del brazo o en el abdomen. Toujeo® ayuda a mantener los niveles de glucosa en sangre controlados y estables durante más de 24 horas. Se puede inyectar en cualquier momento, una vez al día. La inyección debería realizarse a la misma hora todos los días.
Si participa en el estudio, continuará con sus fármacos antidiabéticos no insulínicos habituales. También seguirá su dieta y las recomendaciones sobre el estilo de vida realizadas por su propio equipo sanitario.
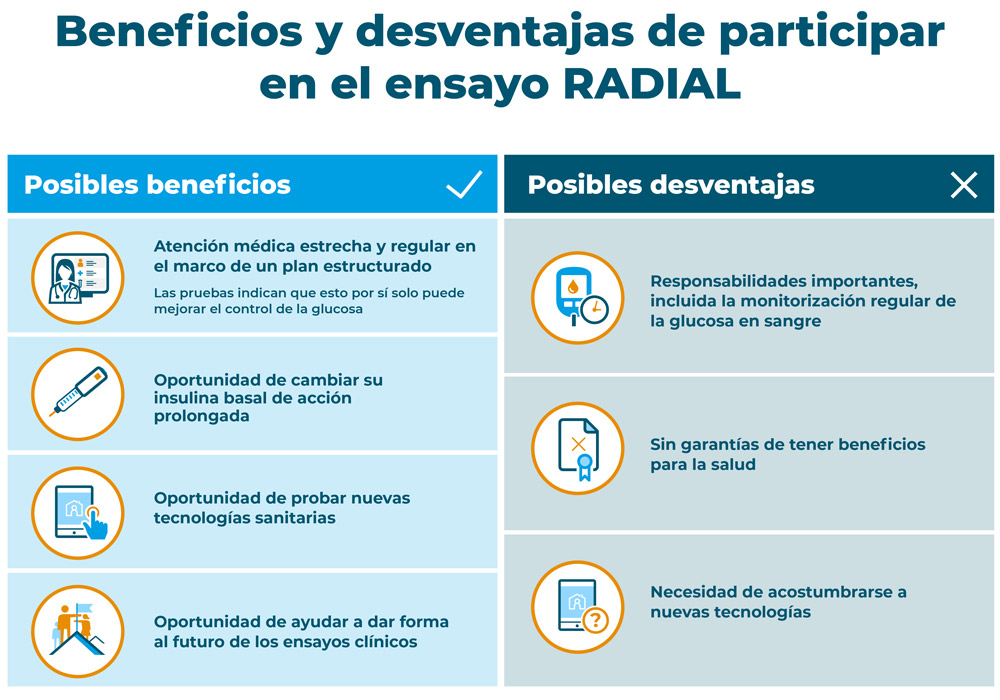
Implicaciones de participar en el estudio
Unirse al estudio RADIAL podría no tener beneficios directos para usted. Sin embargo:
- Estaría ayudando a dar forma al futuro de los ensayos clínicos. Los ensayos descentralizados podrían hacer que la investigación clínica sea más cómoda y más accesible para los participantes. Eso significa que quizá más personas estarían dispuestas a participar en futuras investigaciones.
- Participar en un ensayo clínico podría mejorar su control de la glucosa, debido a la atención médica extra que recibiría. También podría empezar a sentirse empoderado y apoyado para hacer cambios en sus autocuidados.
- Es posible que su control de la glucosa en sangre mejorara debido al cambio a Toujeo®. Las directrices relativas a cómo ajustar la dosis de Toujeo® usted mismo hacen que el control de la glucosa esté en su mano.
- El tratamiento de su diabetes se hará desde la comodidad de su hogar, empleando tecnologías modernas. Ello incluye una tapa «inteligente» para la pluma de insulina que captura automáticamente la dosis, la fecha y la hora de cada inyección. También usará un glucómetro conectado que transmite automáticamente sus mediciones de glucosa en sangre al diario electrónico y al equipo del estudio.

The Trials@Home project has received funding from the Innovative Medicines Initiative 2 Joint Undertaking under grant agreement No 831458. This Joint Undertaking receives support from the European Union’s Horizon 2020 research and innovation programme and EFPIA.
RADIAL Trial does not take any responsibility for any information on external links.
Copyright © 2024